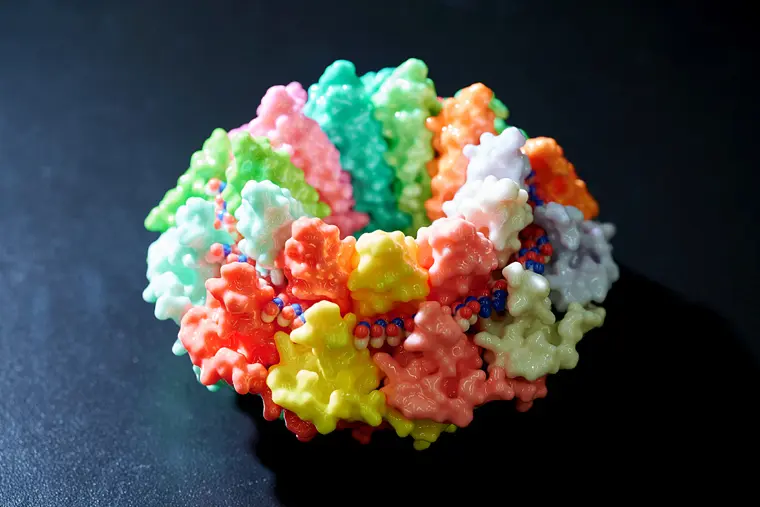
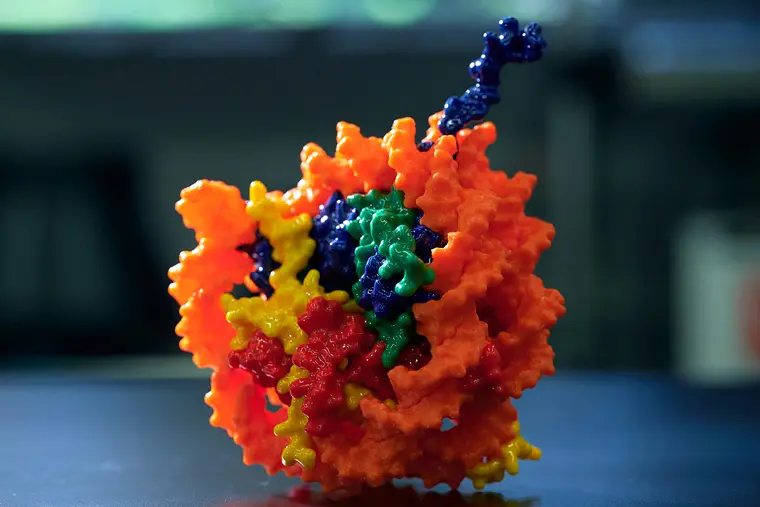
DNAの傷を修復する
メカニズムを解明
香川 亘
理工学部 総合理工学科
教授 /博士(理学)
構造生命科学研究室
香川亘教授が率いる研究チームは、生物が日常的にDNAの損傷を修復する仕組みに焦点を当て、がん細胞の二重鎖切断修復に関わるRAD52タンパク質のDNAとの複合体構造を決定。DNA結合構造を解析。がん治療薬の開発に新たな可能性を切り拓いている。

すべての生物が備える
「遺伝子の傷」を治す仕組み
ヒトは約37兆個の細胞からできており、その一つひとつにゲノムDNAが収納されている。その数は、30億塩基対にのぼる。DNAは、2本の塩基の鎖がらせん状に連なった構造をしており、そこには生物の身体を作るための情報が書き込まれている。DNA配列から読み出された情報を元にさまざまなタンパク質が作られ、細胞の中で働くことで、生命は維持される。DNAが生命の設計図といわれるのはそのためだ。
「しかしゲノムDNAは、細胞の中で常に安定して存在しているわけではなく、日常的にさまざまな傷を受けています。ヒトの場合、その数は細胞1個あたり1日に5万~50万回にも及びます」と説明した香川 亘教授。それほどひんぱんに起こる損傷を放置していては、到底生命を維持できない。そのためヒトを含むあらゆる生物は、遺伝子の傷を治す仕組みを持っているという。
とりわけ近年、世界中の研究者たちが仕組みの解明にしのぎを削っているのが、DNAの両方の鎖が切れてしまう「二重鎖切断」の修復だ。「これはDNA鎖の一方だけが切れる損傷よりもずっと厄介です。二重鎖切断が一つでも修復されないと、細胞死やがんを引き起こす原因になることが知られています。そのため生物は、二重鎖切断を修復する仕組みを何通りも備えています」と言う。
香川教授は、その中でもがん細胞で起こる二重鎖切断を治す仕組みに注目し、その解明に取り組んでいる。そこで焦点を当てるのが、RAD52というタンパク質である。「先行研究で、RAD52タンパク質は、乳がん細胞で二重鎖切断の修復に用いられていることが指摘されています」。だがその仕組みには、いまだ不明な点が多い。香川教授らはこの解明に大きく近づく成果として、RAD52タンパク質がDNAと結合した立体構造を原子レベルで明らかにすることに成功した。
DNAの修復に関立体構造わる
タンパク質の立体構造を解明
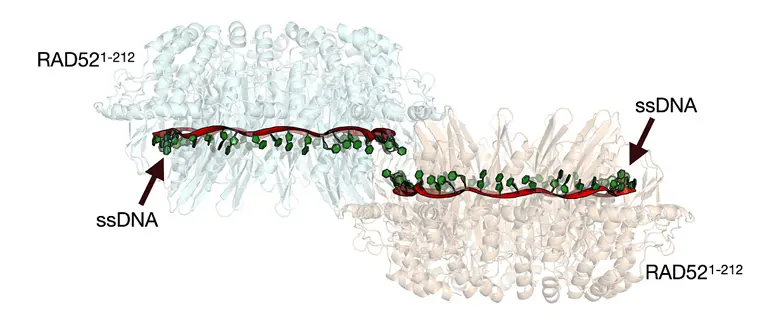
RAD52タンパク質は、11分子からなるリング構造を形成し、リング構造の外周にDNAが収まる大きさの溝が存在することがわかっている。しかし微細なタンパク質を実際に目で見て確かめることはできない。香川教授らは、まずRAD52のDNA複合体を作製してそれを結晶化。得られた結晶に強力なX線を照射し、結晶によって回析されたX線を解析(X線結晶構造解析)することによって、複合体の立体構造を明らかにしようと試みた。
X線結晶構造解析にあたっては、SPring-8(兵庫県・国立研究開発法人理化学研究所)、KEK(つくば市・大学共同利用機関法人高エネルギー加速器研究機構)といった国内屈指の大型放射光施設が利用された。「近年は結晶化プロセスを必要としないクライオ電子顕微鏡解析(東京大学)も利用しています」。こうした最先端の施設・機器を用いて研究は進められている。
「解析の結果、まずRAD52のリング構造の溝に、切断されて単鎖になったDNAが巻き付くように入り込んでいることがわかりました。さらに2個のRAD52が向かい合うように集積し、リング間で単鎖(相補鎖)DNA同士が結合して塩基対を形成するのを促進する仕組みが見えてきました」。これをもとに、RAD52が二重鎖切断を修復する反応モデルを構築した。
「がん細胞での二重鎖切断の修復メカニズムが解明できれば、それを逆手にとって修復を阻害することで、がん細胞を死滅させることも可能になります。つまりがん細胞に特異的に働く治療薬の創製にも可能性が広がります」。現在、他大学との共同研究で、RAD52阻害剤の開発を視野に入れた研究を進めている。
アルツハイマー治療につながる
DNA修復機構を解き明かす
さらに「近年、DNAの二重鎖切断において、RNAを利用したDNA修復の仕組みがあることがわかってきました」と香川教授。
これまでは二重鎖切断を修復する機構として、相同組換えがよく知られてきた。DNAの切断箇所と、類似または同じ塩基配列を鋳型として複製し、欠損部に当てはめて復元する方法だ。これに対し、タンパク質をつくるプロセスで、DNAを転写したRNAを鋳型にして欠損した塩基配列を正確に修復する機構があるという。「相同組換えは、分裂細胞で起こるのに対し、心筋細胞や神経細胞といった非分裂細胞では、RNAを利用した修復が重要な役割を果たすと考えられています。面白いことに、ここにRAD52が関わることが分かってきました」と言う。
香川教授らは、RNAを利用したDNAの修復反応を試験管内で再現。そこにRAD52タンパク質を導入すると、これが触媒として働き、DNA修復が促進されることを確かめた。一方で相同組換え反応で働くタンパク質をRNAによる修復反応に導入しても、修復は促進されなかった。「このことから、RAD52は、RNAを利用したDNA修復機構に特異的に働くのではないかと推測しています。これを確かめるため、今後さらに検証を進めていくつもりです」
RNAを利用したDNA修復メカニズムが解明できれば、アルツハイマーや認知症といった、いまだ根本的な治療法のない脳や神経疾患の治療に、光明を見出せるかもしれない。香川教授の研究に、大きな期待がかかっている。
香川 亘
理工学部 総合理工学科
教授 /博士(理学)
構造生命科学研究室

専門分野
構造生物化学、分子生物学、機能生物化学
キーワード
X線結晶構造解析、タンパク質・核酸複合体、相同組換え修復、クロマチン、ヌクレオソーム
研究室HP
構造生命科学研究室 明星大学 香川研究室教員情報
明星大学教員情報 香川 亘2024年3月掲載
*内容・経歴は取材もしくは執筆時のものです。